Tabla de contenidos
¿Qué es la densidad?
La densidad se define como la cantidad de materia que hay en un volumen determinado.
También se puede definir como el grado de compactación de una sustancia, así por ejemplo el oro es más denso que el algodón, o el hierro es más denso que una nube.
Historia
El estudio de la densidad de los objetos es tan antiguo como el mismo ser humano. En la antigüedad se hacía transporte de mercancías a través de diferentes lugares y allí fue necesario conocer sobre esta propiedad.
Cuando los transportadores llenaban sus carretas podían analizar que algunos productos eran «más pesados» para llevar esas cargas «más pesadas» se necesitaba no de uno sino de dos o más caballos.
Con el paso del tiempo los mercaderes lograron identificar cuáles eran esos productos y cobraban más por su transporte, entre más denso fuera el material, mayores cobros hacían puesto que necesitaban de más animales y los gastos se hacían mayores.
Sin embargo el suceso que más relevancia tiene históricamente sucedió en el año 250 AC, en esa fecha se le encargó al matemático griego Arquímedes determinar si la corona del rey de Siracusa era completamente en oro.
Existía una desconfianza por parte del rey en que la corona podía tener una mezcla de metales y él había pagado por oro puro.
Arquímedes intentó resolver el enigma de una forma matemática, la masa de la corona era fácil de determinar pero el volumen de la corona no. La corona tenía una forma irregular por lo que se hacía difícil conocer el volumen real a partir de figuras geométricas.
Meditando en la solución del ejercicio Arquímedes se sumergió a tomar un baño regando una cantidad de agua allí se dio cuenta que el volumen de agua regada aumentaba cuando se sumergía un cuerpo más grande.
De este modo si sumergía la corona y la misma cantidad en masa de oro ambas deberían regar la misma cantidad de agua.
Si la corona tenía un metal diferente al oro, por ejemplo plata, al ser un material menos densos va a ocupar más volumen por lo que más agua se va a regar, al llegar a esta conclusión Arquímedes salió desnudo por las calles gritando ¡eureka! que significa «lo encontré»
Finalmente cuando se hizo el experimento el artesano estaba engañando al rey por lo que fue ejecutado.
¿Qué es la densidad en química y en física?
En química y en física se cataloga como una propiedad intensiva, es la relación que hay entre la masa de un cuerpo y el volumen que ocupa y se representa con la letra griega rho (ρ).
¿Cuál es la fórmula ?
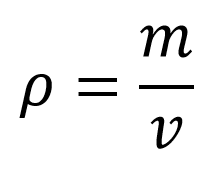
Teniendo en cuenta que la densidad relaciona la masa y el volumen a partir de la ecuación se puede determinar que:
- En un volumen determinado a mayor masa, mayor densidad
- Teniendo una masa determinada, a mayor volumen, menor densidad
Densidad absoluta o densidad real
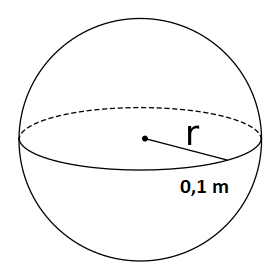
Es la densidad que tiene un cuerpo o sustancia cuando se analiza su masa y su volumen, por ejemplo calculemos si se tiene una esfera que tiene una masa de 10 kg y tiene un radio de 0,1 metros
Se procede a calcular
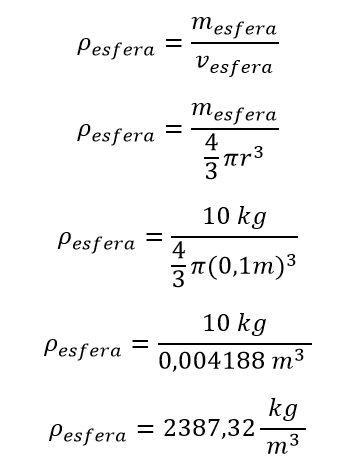
Densidad aparente
Es la densidad que tienen los cuerpos cuando se acumulan entre sí y quedan espacios vacíos, depende de la compactación que tengan los cuerpos, entre menos compactación más espacios va a haber vacíos.
Vamos a tomar el mismo ejemplo anterior con la esfera (2387 kg/m3) si se mira individualmente, pero ¿qué sucede si juntamos dos esferas y queremos calcular la nueva densidad?
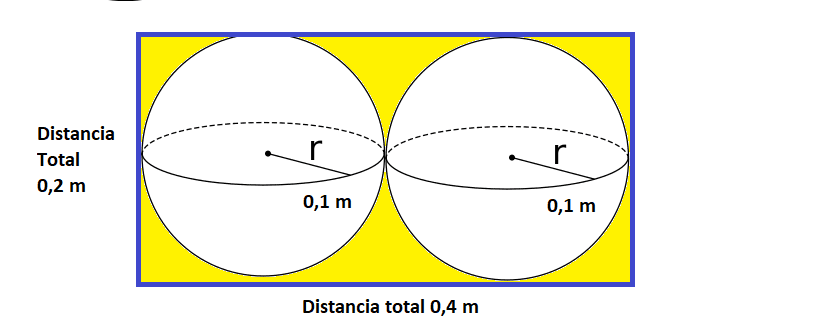
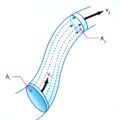
Cuando se analizan dos esferas pegadas, se puede evidenciar que el volumen que ocupan no es el volumen de la esfera por dos sino que se observa que quedan espacios vacíos mostrados en color amarillo.
El espacio en la práctica que ocupan las dos esferas será su volumen más el volumen de los espacios amarillos ya que no se pueden rellenar con más esferas.
Es decir que la esfera vista desde la práctica está ocupando un volumen que es un cubo de 0,2 m x 0,2 m x 0,2 m

La densidad aparente siempre es menor o igual que real, para este caso la densidad real de la esfera es 2387,32 kg/m3 pero cuando se analiza la aparente es de solo 1250 kg/m3.
Densidad relativa
Es la densidad de una sustancia dividida entre la densidad de una sustancia conocida, en la mayoría de líquidos se utiliza como referencia el agua.
Es una medida adimensional, es decir que no tiene unidades a diferencia de la densidad aparente o la real que manejan las unidades kg/m3.
La ecuación es:
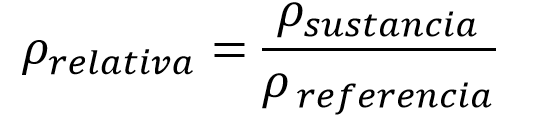
Ejemplo:
La densidad relativa de un líquido es de 0,95 con respecto al agua ¿cuál es la densidad absoluta del líquido?

Densidad y flotabilidad
Para que un objeto pueda flotar su densidad debe ser menor que la del agua, en caso contrario el objeto se hundirá, si la densidad del objeto y del agua son iguales este se mantendrá en el medio sin hundirse y sin flotar

Ejercicios resueltos densidad
Ejercicio 1:
¿Cuál es la densidad de una tabla de madera cuyas medidas son 1,5 m de largo, 0,25 m de ancho y 0,05 m de gruesa si tiene una masa de 50 kg?
Solución
Lo primero que se debe determinar es la ecuación
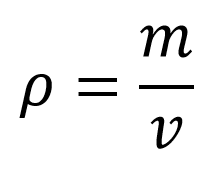
Para poder calcular la densidad se necesita de la masa y del volumen de la tabla, en este ejercicio se especifica la masa sin embargo se debe calcular el volumen.
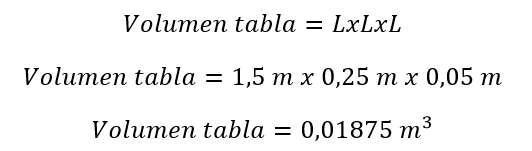
Una vez se conoce la masa y el volumen se procede a calcular la densidad
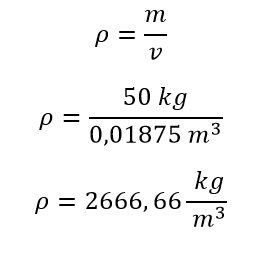
Ejercicio 2
Una sustancia que tiene una densidad de 1600 kg / m3 ocupa un espacio de 2 m3 ¿Cuánta masa de esa sustancia hay?
Solución
Lo primero que se debe determinar es la ecuación de la densidad
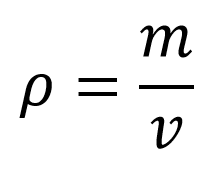
Debido a que se conoce la densidad y el volumen de la sustancia necesitamos despejar la masa, una vez despejada la masa se reemplazan los valores y se hacen los cálculos para saber la cantidad.
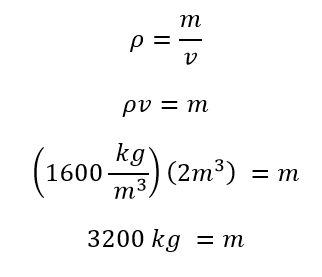
Ejercicio 3
Se desea guardar 5000 kg de una sustancia que tiene una densidad de 800 kg/m3 ¿Cuánto espacio ocupará?
Solución
Lo primero que se debe determinar es la ecuación de la densidad
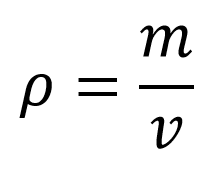
Una vez se tiene la ecuación de la densidad, se debe despejar el volumen y reemplazar los valores para poder calcularlo.
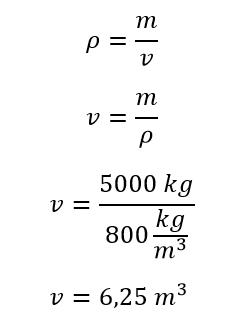
¿Cómo se mide la densidad de las sustancias?
Existen diferentes maneras de determinar la densidad de las sustancias dependiendo el estado y las características generales, las principales son:
Método de empuje
Consiste en utilizar el principio de Arquímedes para la determinación de la densidad de un sólido, lo primero es que se toma la masa del sólido, este valor lo llamaremos masa sólido (ms)

Una vez se conoce la masa del sólido se procede a tomar la masa de un vaso con agua, este valor lo llamaremos m1

Luego se sumerge el sólido dentro del vaso con agua y vuelve a tomarse la masa en la balanza, este valor lo llamaremos m2

De este modo la densidad del objeto se calcula mediante la fórmula
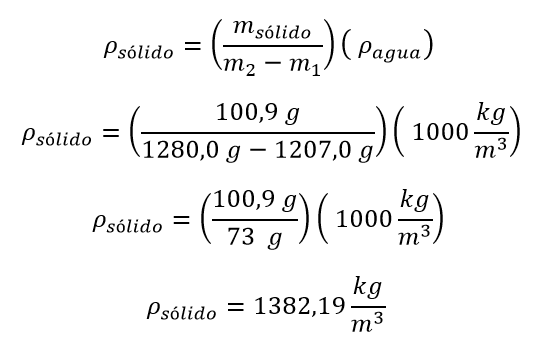
Método del picnómetro
El picnómetro es un envase de vidrio o acero inoxidable que tiene una tapa con un fino espacio capilar en la parte superior lo que permite obtener volumenes con una gran precisión.

El uso del picnómetro para determinar la densidad de un líquido es muy habitual, ya que es económico y fácil de utilizar.
Lo primero que se debe hacer es tomar el peso del picnómetro (esta medida se llamará masa del picnómetro) se debe tener cuidado que se encuentre totalmente seco y sin material externo que pueda influir en un aumento de peso.
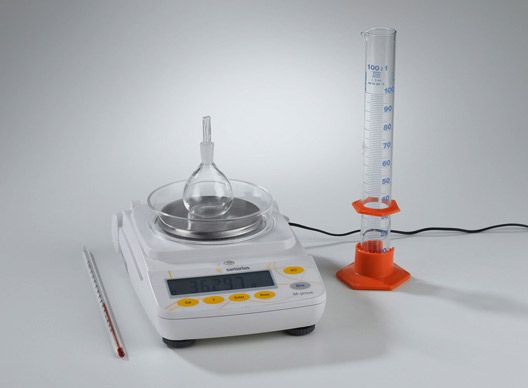
Luego se llena el picómetro con agua y vuelve a pesarse (esta medida se llamará masa del picnómetro + agua)
Finalmente se vacía, se seca el picnómetro y se llena nuevamente con la sustancia a la cual le queremos medir la densidad (aceite, alcohol o cualquier sustancia líquida) y se vuelve a tomar el peso (esta medida se llamará masa de picnómetro + líquido), la densidad de la sustancia de interés se calcula a partir de la ecuación
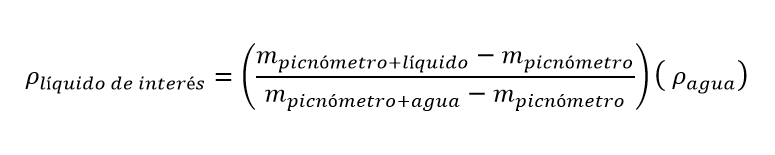
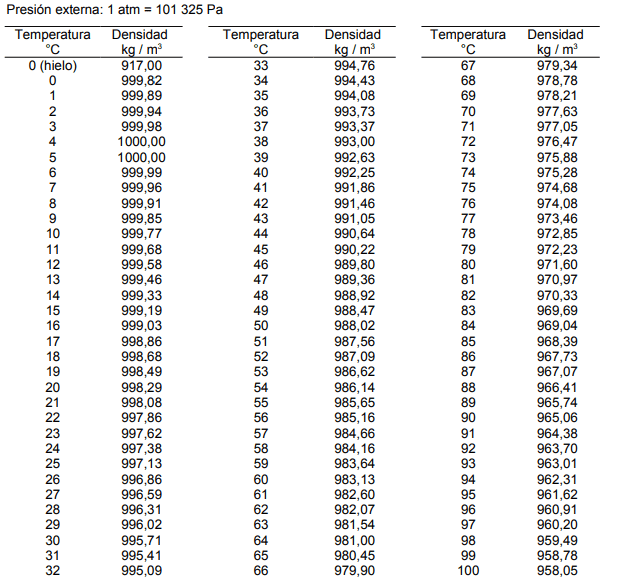
La densidad del agua va a depender de la temperatura a la cual se realizó la medición de las masas y se obtendra de la siguiente tabla
Tabla de densidad de agua a diferentes temperaturas
Ejemplo de cálculo de densidad con un picnómetro
Se desea medir la densidad de un líquido desconocido a través del uso de picnómetro, se pesa el picnómetro y tiene una masa de 45 gramos, luego se llena con agua y termina pesando 90 gramos, se vacía, se seca y se llena con el líquido desconocido y al pesar da como resultado 87 gramos, si todo el experimento se realizó a 20°C ¿Cuál es la densidad de la sustancia desconocida?
Solución
Lo primero que se debe hacer es plantear la ecuación con picnómetro
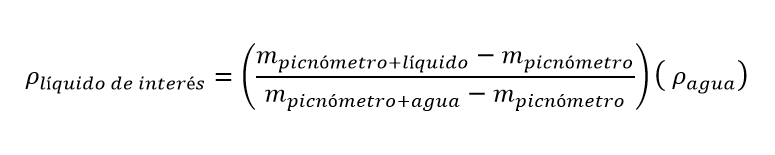
Se reemplazan los valores de las masas de acuerdo con el enunciado y se busca la densidad del agua en la tabla a 20°C que es 998,29 kg/m3

Método del densímetro
El densímetro es un equipo que permite hacer la determinación de la densidad de un líquido de forma experimental, fácil y rápida.
Simplemente se introduce el densímetro dentro del líquido y este marcará el valor de la densidad.
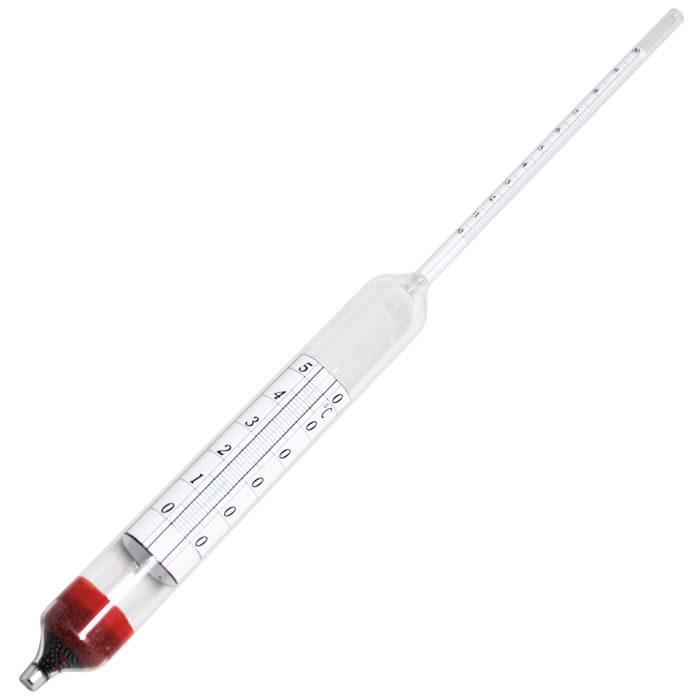
La única recomendación que se debe tener en cuenta con el uso del densímetro es que el valor de la densidad que arroja es densidad relativa con respecto al agua, entonces si marca 1,2 la densidad será de 1200 kg/m3
Recomendaciones en la medición de las densidades
- Minimizar al máximo los errores en el pesaje de la muestra, calibrar la balanza y operarla cuando no hayan corrientes de viento
- Evitar la generación de burbujas ya que el volumen dentro es de aire y no de la sustancia que se quiere analizar lo que lleva a errores en la medición
- Evitar cambios bruscos de temperatura debido a que algunos líquidos se pueden expandir o contraer afectando el resultado
- Establecer las unidades de medida para no confundir gramos con kilogramos o litros con mililitros
¿Puede cambiar la densidad de una sustancia?
Los materiales sólidos y líquidos se considera que tienen una densidad constante, sin embargo algunas sustancias cambian de densidad con cambios en la temperatura, por ejemplo el agua como se puede ver en la tabla:
- Desde los 4°C y a medida que se calienta disminuye
- Debajo de los 4°C cuando empieza a convertirse en hielo disminuye ( el hielo es menos denso que el agua y por eso flota)
Aunque los cambios son mínimos es importante conocerlos , cuando se habla de sistemas con varios objetos es más fácil determinar los cambios, algunos ejemplos son:
Aumento
Se tiene una caja vacía y se le mide la densidad, después se le van añadiendo rocas a la caja, en este caso el volumen no cambia puesto que la caja no se agranda ni se encoge.
La masa aumenta cada vez que una roca nueva se guarda, para este ejemplo la densidad del sistema cada vez se hace mayor puesto que la masa se hace mayor a medida que el volumen se mantiene constante.
Disminución
Se tiene un kilogramo de agua en estado líquido y se empieza a calentar hasta lograr el punto de ebullición.
Al cambiar al estado gaseoso la masa sigue siendo un kilogramo pero el espacio que ocupa va a ser mayor puesto que el gas ocupa un mayor volumen que el líquido, de este modo se puede disminuir la densidad en un sistema.
Usos de la densidad
- Determinación de pureza de diferentes sustancias: por ejemplo la determinación de oro por parte de Arquímedes con la corona
- Determinación de flotabilidad o no de cuerpos: diseño de estructuras como barcos, submarinos entre otros
- Certificación de calidad de productos: determinación en la leche para saber que no se le ha agregado agua para rendirla
- Determinación de espacios en bodegas: cuántos m3 se necesitarán para almacenar una cantidad determinada de un material
Densidad de sustancias
Conociendo el concepto quizás te preguntes ¿Cuál es la densidad del agua?, ¿Cuál es la del aire?, ¿cuál es la del mercurio? o ¿cuál es la del oro? debido a esto tenemos una tabla con las principales sustancias.
| Sustancia o material | Densidad (kg/m3) | (g/ml) | (g/cm3) |
| Agua | 1000 | 1 | 1 |
| Aire | 1,22 | 0,00122 | 0,00122 |
| Mercurio | 13690 | 13,69 | 13,69 |
| Oro | 19320 | 19,32 | 19,32 |
| Hierro | 7874 | 7,874 | 7,874 |
| Alumunio | 2700 | 2,7 | 2,7 |
| Plomo | 11300 | 11,3 | 11,3 |
| Alcohol | 789 | 0,789 | 0,789 |
| Cobre | 8960 | 8,96 | 8,96 |
| Orina | 1030 | 1,03 | 1,03 |
| Hielo | 916,8 | 0,9168 | 0,9168 |
| Madera | 500 | 0,5 | 0,5 |
| Oxígeno | 1,43 | 0,00143 | 0,00143 |
| Ácido Clorhídrico HCl (gas) | 1,49 | 0,00149 | 0,00149 |
| Ácido Clorhídrico HCl (liq) | 1190 | 1,19 | 1,19 |
| Gasolina | 680 | 0,68 | 0,68 |
| Vidrio | 2500 | 2,5 | 2,5 |
| Dióxido de Carbono CO2 | 1,98 | 0,00198 | 0,00198 |
| Leche | 1032 | 1,032 | 1,032 |
| Gas Natural | 0,743 | 0,000743 | 0,000743 |
| Titanio | 4540 | 4,54 | 4,54 |
| Nitrógeno | 1,25 | 0,00125 | 0,00125 |
| Hidrógeno | 0,071 | 0,000071 | 0,000071 |
| Vinagre | 1050 | 1,05 | 1,05 |
| Metanol | 792 | 0,792 | 0,792 |
| Glicerina | 1260 | 1,26 | 1,26 |
| Cemento | 2800 | 2,8 | 2,8 |
| Bronce | 890 | 0,89 | 0,89 |
| Diésel | 850 | 0,85 | 0,85 |
| Harina de trigo | 498 | 0,498 | 0,498 |
| Zinc | 714 | 0,714 | 0,714 |
| Grava | 1550 | 1,55 | 1,55 |
| Butano | 573 | 0,573 | 0,573 |
| Tierra | 5510 | 5,51 | 5,51 |
| Miel | 1402 | 1,402 | 1,402 |
| Hidróxido de Sodio NaOH | 2130 | 2,13 | 2,13 |
| Sangre | 1070 | 1,07 | 1,07 |


me pareció una muy buena explicación, sobre todo para mi que he vuelto a retomar los estudios después de muchosssss….años. gracias.